近十几年以来,美国最高法院围绕35 USC §101(本文也称为"101法条")做出了一系列判决,对电学领域和生物医药领域申请人的专利保护策略产生了极大的影响。在生物医药领域中,用作疾病诊断标志物的基因产物、疾病诊断的方法和天然的益生菌等研究成果都具备重大的商业价值。然而,在上述一系列判决的影响下,这些研究成果在商业化之前在美国面临着如何获得充分专利保护的难题。在美国当前的专利审查实践下,申请人通常需要牺牲一部分保护范围才能够使权利要求符合101法条的规定并获得专利授权,而牺牲的保护范围势必会影响到专利授权后的可维权性和授权专利的价值。因此,如何应对美国101法条的审查实践变化,特别是如何避免授权专利的保护范围和价值受到负面影响或者使此类负面影响尽可能降低,是申请人所面临的挑战和难题。本文对101法条的审查实践变化过程、变化原因和现状进行介绍和分析,并提供一些应对思路,供生物医药领域的申请人参考。
一、101法条的规定
Whoever invents or discovers any new and useful process, machine, manufacture, or composition of matter, or any new and useful improvement thereof, may obtain a patent therefor, subject to the conditions and requirements of this title.
任何新的且有用的方法、机器、制造物或物质组合,或者对前述内容所做出的任何新的且有用的改进,都可以获得专利。
35 USC §101(本文也称为"101法条")属于专利适格性(Patent Eligibility)的规定(专利适格性是指某项发明或发现是否符合专利法规定的条件,从而可以被授予专利权)。该法条规定了可以被授予专利权的四种主题,即,方法(Process)、机器(Machine)、制造物(Manufacture)以及物质成分(Composition of Matter)。美国在立法初始,为了鼓励大众进行发明创造,101法条并没有明确规定任何不可以被授予专利权的主题,在四种可以被授予专利权的主题范围下也并没有进行更进一步的限定。
但是,在多年来法院所做出的判决影响下,101法条的审查实践逐渐发生变化,并逐渐演变形成了三大司法例外(Judicial exception),即,自然法则(Laws of Nature)、自然现象(Natural Phenomenon)和抽象概念(Abstract Ideas)。其中,自然现象包含了天然产物(Products of Nature)。
二、101法条审查实践的变化过程、变化原因以及现状
在上述司法例外形成的过程中,2010年至2014年是一个非常重要的时间点。在此期间,美国最高院在不同领域以专利不符合101法条为理由连续做出了多件无效判决,并将"101问题"推上了风口浪尖。其中,最受关注的4件判决分别是涉及商业方法的Bilski案(Bilski v. Kappos (2010))、涉及计算机软件的Alice Corp案(Alice Corp. Pty. Ltd. v. CLS Bank Int'l (2014))、涉及疾病诊断方法的 Mayo案(Mayo Collaborative Services v. Prometheus Labs. Inc. (2012))以及涉及天然基因产物的Myriad 案(Assoc. for Molecular Pathology v. Myriad Genetics (2013))。在连续多件判决的影响下,USPTO不仅快速发布了暂行指南,对101法条界定范围内的可授权主题进行了限制,还随之推出了判断权利要求是否符合101法条的"两步法"原则,并且这一判断原则也沿用至今。以对生物医药领域中天然产物类专利具有深远影响的Myriad 案(Assoc. for Molecular Pathology v. Myriad Genetics (2013))为例,101法条下审查实践的变化情况可见一斑。
Myriad公司发现了能够用于诊断乳腺癌或卵巢癌的基因BRCA1和BRCA2,在鉴定出了基因BRCA1和BRCA2的位置和序列后,申请了一系列专利 (US Patent Nos. 5747282, 5693473和5837492)。在获得相应的专利权之后,Myriad公司对使用这两个基因进行检测的研究所和医疗团队提起了诉讼,并垄断了与这两个基因相关的任何检测项目。Myriad公司的垄断行为不仅使得科研人员无法对BRCA1和BRCA2基因进行深入研究,也使得患者不得不承受高昂的癌症检测费用。在这种情况下,美国分子病理协会(Molecular Pathology)联合医院等众多机构和患者团体共同对Myriad公司提出了无效请求。显然,该诉讼案件背后涉及到了社会大众、科研人员以及生物医药领域的研发企业等多方利益。
该案件从地方法院一直被诉至最高法院,争论的焦点始终在于权利要求1所保护的"BRCA1的核苷酸序列"是否符合101法条的规定。最终,最高院认为权利要求1违反了101法条的规定,因此权利要求1也被宣告无效。最高院给出的理由是:在专利权人发现BRCA1基因的位置及其核苷酸序列之前,该基因的位置及其核苷酸序列在自然界就早已存在。因此,专利权人没有创造任何东西。可以肯定的是,专利权人发现了一个重要且有用的基因,但是将该基因与周围的遗传物质分开并不是一项发明行为。
值得注意的是,在此判决之前,对于涉及天然产物的专利申请来说,101法条下的反对意见并不是一个难以克服的问题。通常,在权利要求的主题中加入"分离的(isolated)"或"纯化的(purified)"就可以将所要保护的产品与自然界中存在的物质区分开来。因为在当时看来,自然界中存在的物质既不是分离的,也不是纯化的。然而,在该判决中,这种应对方式显然不被最高院认可。该判决不仅改变了生物医药领域的申请人一贯的专利保护策略,也对生物医药领域的专利申请带来了新的障碍和困难。
三、101法条的"两步法"测试
在Alice案和Mayo案之后,USPTO在2014年发布了《专利主题适格性指南》,并提供了判断权利要求是否属于可授权主题的"两步法"测试。2019年,USPTO公布了《专利主题适格性指南2019修订版》,并对该"两步法"测试进行了细化。以下为细化后的"两步法"测试的流程图和具体步骤:
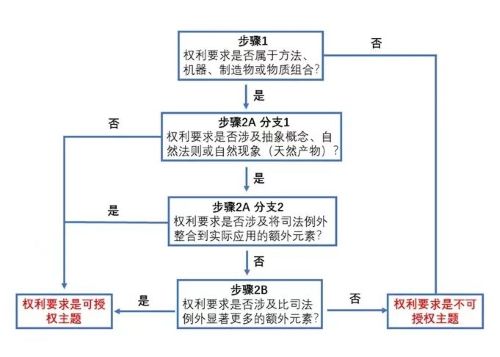
步骤1:判断权利要求是否属于方法、机器、制造物或物质组合;
步骤2A:该步骤包括分支1和分支2;其中,
分支1:判断权利要求是否涉及抽象概念、自然法则或自然现象(包括自然产物)?如果权利要求涉及自然产物,则需要进行"明显区别特征分析(Markedly Different Characteristic Analysis)";
分支2:判断权利要求是否涉及将司法例外整合到实际应用的额外元素(additional element);
步骤2B:判断权利要求是否涉及比司法例外显著更多(Significantly more)的额外元素(additional element)。
其中,"明显区别特征分析",是指判断权利要求所涉及的产品相对于自然产生的对应产品而言,结构、功能和/或其他属性是否有差别;具体地,包括:
1)生物或药理功能或活性,例如,细菌感染豆科植物的能力,或核酸的蛋白质编码信息;
2)化学和物理性质,例如,化合物的碱度,或金属的延展性;
3)表型,包括功能和结构特征,例如,生物的形状、大小、颜色;
4)化学的、遗传的或物理的结构和形式,例如,质粒在细菌细胞中的物理存在,或化学物质的晶体形式。
也就是说,在"两步法"测试中,需要先对权利要求的保护主题进行判断(步骤1);如果其属于方法、机器、制造物或物质组合,则继续判断权利要求是否涉及司法例外,即,抽象概念、自然法则或自然现象(步骤2A中的分支1);如果权利要求涉及司法例外,则需要继续判断权利要求是否涉及将司法例外整合到实际应用的额外元素(步骤2A中的分支2);如果权利要求不涉及将司法例外整合到实际应用的额外元素,则需要继续判断权利要求是否具备比司法例外显著更多(Significantly more)的额外元素(步骤2B)。
换言之,在上述步骤中,如果权利要求一旦被判定为涉及司法例外,则需要在步骤2A中的分支2和步骤2B中先后两次对额外元素进行判断,以确定权利要求是否属于可授权主题。因此,在"两步法"测试中,权利要求中是否包含额外元素以及包含什么样的额外元素显得尤为重要。
四、101法条在生物医药领域中的审查示例和分析
对于生物医药领域来说,在"两步法"测试过程中可能涉及司法例外的主题主要有两大类,即,天然产物类主题(其涉及司法例外中的自然现象),和诊断方法类主题(其涉及司法例外中的自然法则/抽象概念)。具体来说,任何从自然界中新分离、提取或纯化出来的核酸分子、蛋白、细胞、微生物(例如,益生菌)、植物提取物(例如,柚子汁)和化合物(例如,亚马逊酸)都可能被视为天然产物,从而涉及101法条测试过程中的司法例外。而任何利用天然存在的规律和/或现象对疾病进行预测、判断和/或检测的方法都可能被视为自然法则/抽象概念,从而涉及101法条测试过程中的司法例外。
结合上述的"两步法"测试,以下通过几个不同类型的示例对可授权主题和不可授权主题进行具体分析。
示例1 核酸分子
1. Isolated nucleic acid comprising SEQ ID NO: 1.
该权利要求不具有专利适格性
理由:权利要求1涉及从自然界中分离出的基因W(序列如SEQ ID NO:1所示),该基因与其自然状态下的天然对应物(3号染色体上的基因W)没有明显不同,因此属于司法例外中的"自然产物",因此权利要求1属于不可专利主题。
2. A vector comprising an isolated nucleic acid comprising SEQ ID NO: 1 and a heterologous nucleic acid sequence.
该权利要求具有专利适格性
理由:权利要求2涉及一种载体,该载体包含基因W(SEQ ID NO:1)以及来自另一种生物的序列。这两种序列的组合在自然界中不会天然地组合在一起,因此该载体具有与天然存在的核酸不同的遗传结构和序列,即不同的结构特征。这种不同的结构特征使得该载体具有了显著不同的特征,因此该载体不属于"自然产物"的司法例外。因此权利要求2属于可专利主题。
示例2 柚子果实
1. A method comprising providing a pomelo fruit.
该权利要求不具有专利适格性
理由:虽然该权利要求是一项方法权利要求,但其撰写方式使其与产品权利要求,即,柚子果实本身在实质上没有区别。由于说明书中没有表明所要求保护的果实具有与柚子树上的天然果实任何不同的特征(结构、功能或其他方面)。因此,权利要求1的柚子果实与自然界中的水果没有明显不同的特征,属于"自然产物"的司法例外。因此权利要求1属于不可专利主题。
2. A beverage composition comprising pomelo juice and an effective amount of an added preservative.
该权利要求具有专利适格性
理由:该权利要求是一种基于自然的产品,即天然存在的物质(柚子汁)与添加的防腐剂的组合物。因此,需要分析以确定其在自然状态下是否与任何天然存在的对应物具有显著不同的特征。说明书指出,防腐剂的来源可以是天然的或非天然的。但无论其来源如何,当有效量的防腐剂与柚子汁混合时,防腐剂会影响果汁,使其与天然果汁相比(几天内就会变质),以更慢的速度变质(几周内才会变质)。因此,所要求保护的组合物的这种特性(较慢的变质速度)在本质上明显不同于果汁本身的特性。因此,该组合物具有明显不同的特征,因此其不属于"自然产物"的司法例外。因此权利要求2属于可专利主题。
示例3 诊断方法
1. A method of diagnosing julitis in a patient, said method comprising:
a. obtaining a plasma sample from a human patient;
b. detecting whether JUL-1 is present in the plasma sample by contacting the plasma sample with an anti-JUL-1 antibody and detecting binding between JUL-1 and the antibody; and
c. diagnosing the patient with julitis when the presence of JUL-1 in the plasma sample is detected.
该权利要求不具有专利适格性
理由:该权利要求列举了一系列检测血浆样本中JUL-1的存在的步骤。因此,该权利要求涉及一种方法,属于法定发明类别之一(步骤1:是)。进一步,在步骤c中,其描述了当检测到血浆样本中JUL-1的存在时诊断患者患有julitis(一种自身免疫性疾病)。即,步骤c描述了患者血浆中JUL-1与julitis之间的相关性或关系。这一步骤属于司法例外,因为这种相关性属于自然法则(参见,美国最高法院在Mayo案中的认定)。因此,该权利要求涉及司法例外(步骤2A分支1:是),其可以被称为自然法则、抽象概念或两者兼而有之。此处应注意,尽管该权利要求列举了几个基于自然现象的产品(例如,血浆样品和JUL-1),但该权利要求作为一个整体侧重于检测JUL-1是否存在于血浆样品中的过程,而不是侧重于产品本身。因此,不需要对所列举的基于自然现象的产品进行明显区别特征分析。
接下来,对整个权利要求进行分析,以确定是否有任何元素或元素组合足以使权利要求明显超过司法例外情况。除了自然法则,该权利要求还描述了从人类患者获得血浆样品的步骤(步骤a),以及通过使血浆样品与抗JUL-1抗体接触并检测JUL-1和抗体之间的结合来检测JUL-1是否存在于血浆样品中的步骤(步骤b)。对于诊断领域的人员来说,获取样本以进行测试是一项众所周知的常规活动。此外,检测血浆样本中是否存在JUL-1仅描述了使用任何通用抗JUL-1抗体的检测技术。这种高度普遍性的描述对于步骤b没有任何有意义的限制。并且,众所周知,获取样本和检测等步骤本身并不能自动赋予针对抽象概念的可授权资格(例如,参见Alice案)。因此,权利要求1作为一个整体并没有明显超过司法例外(步骤2A分支2、步骤2B:否)。因此权利要求1属于不可专利主题。
2. A method of diagnosing julitis in a patient, said method comprising:
a. obtaining a plasma sample from a human patient;
b. detecting whether JUL-1 is present in the plasma sample by contacting the plasma sample with a porcine anti-JUL-1 antibody and detecting binding between JUL-1 and the porcine antibody; and
c. diagnosing the patient with julitis when the presence of JUL-1 in the plasma sample is detected.
该权利要求具有专利适格性
理由:该权利要求列举了一系列检测血浆样本中JUL-1的存在的步骤。因此,该权利要求涉及一种方法,属于法定发明类别之一(步骤1:是)。进一步,由于权利要求2描述了与权利要求1相同的相关性步骤(步骤c),而如上所述这是一个自然法则和/或抽象概念。因此该权利要求属于司法例外(步骤2A分支1:是)。尽管该权利要求列举了几个基于自然现象的产品(血浆样品、JUL-1和抗体),但没有必要进行明显区别特征分析(原因同权利要求1)。
接下来,对整个权利要求进行分析,以确定是否有任何元素或元素组合足以使权利要求明显超过司法例外情况。除了自然法则,该权利要求还描述了从人类患者获得血浆样品的步骤(步骤a),以及通过使血浆样品与猪抗JUL-1抗体接触并检测JUL-1和抗体之间的结合来检测JUL-1是否存在于血浆样品中的步骤(步骤b)。与上述权利要求1的相同的原因,获取样本以进行测试是一项众所周知的常规活动。然而,步骤b还需要使用猪抗JUL-1抗体进行检测。在本申请之前,该领域的大多数科学家都知道猪抗体在兽医治疗中的用途。但值得注意的是,没有证据表明猪抗体被常规或经常性地用于检测人类蛋白质,如JUL-1。因此,该权利要求中使用猪抗体检测JUL-1是一个非常规的步骤。无论是单独考虑还是与其他额外元素综合考虑,使用猪抗JUL-1抗体检测JUL-1的步骤总体上远远超过了司法例外的情况(步骤2B:是)。因此权利要求2属于可专利主题。
3. A method of diagnosing julitis in a patient, said method comprising:
a. obtaining a plasma sample from a human patient;
b. detecting whether JUL-1 is present in the plasma sample by contacting the plasma sample with antibody mAb-D33 and detecting binding between JUL-1 and antibody mAb-D33; and
c. diagnosing the patient with julitis when the presence of JUL-1 in the plasma sample is detected.
该权利要求具有专利适格性
理由:该权利要求列举了一系列检测血浆样本中JUL-1的存在的步骤。因此,该权利要求涉及一种方法,属于法定发明类别之一(步骤1:是)。进一步,由于权利要求3描述了与权利要求1相同的相关性步骤(步骤c),而如上所述这是一个自然法则和/或抽象概念。因此该权利要求属于司法例外(步骤2A分支1:是)。尽管该权利要求列举了几个基于自然现象的产品(血浆样品、JUL-1和抗体),但没有必要进行明显区别特征分析(原因同权利要求1)。
接下来,对整个权利要求进行分析,以确定是否有任何元素或元素组合足以使权利要求明显超过司法例外情况。除了自然法则,该权利要求还描述了从人类患者获得血浆样品的步骤(步骤a),以及通过使血浆样品与抗体mAb-D33接触并检测JUL-1和抗体之间的结合来检测JUL-1是否存在于血浆样品中的步骤(步骤b)。与上述权利要求1的相同的原因,获取样本以进行测试是一项众所周知的常规活动。然而,步骤b还需要使用特异性抗JUL-1抗体(mAb-D33,其是由申请人制备的)进行检测。在本申请之前,抗体mAb-D33不是常规用于检测JUL1蛋白的抗体。因此,该权利要求中使用mAb-D33检测JUL-1是一个非常规步骤。无论是单独考虑还是与其他额外元素综合考虑,使用mAb-D33检测JUL-1的步骤总体上远远超过了司法例外的情况(步骤2B:是)。因此权利要求3属于可专利主题。
4. A method of diagnosing and treating julitis in a patient, said method comprising:
a. obtaining a plasma sample from a human patient;
b. detecting whether JUL-1 is present in the plasma sample;
c. diagnosing the patient with julitis when the presence of JUL-1 in the plasma sample is detected; and
d. administering an effective amount of topical vitamin D to the diagnosed patient.
该权利要求具有专利适格性
理由:该权利要求列举了一系列检测血浆样本中JUL-1的存在的步骤。因此,该权利要求涉及一种方法,属于法定发明类别之一(步骤1:是)。进一步,由于权利要求4描述了与权利要求1相同的相关性步骤(步骤c),而如上所述这是一个自然法则和/或抽象概念。因此该权利要求属于司法例外(步骤2A分支1:是)。尽管该权利要求列举了几个基于自然现象的产品(血浆样品、JUL-1和抗体),但没有必要进行明显区别特征分析(原因同权利要求1)。
接下来,对整个权利要求进行分析,以确定是否有任何元素或元素组合足以使权利要求明显超过司法例外情况。除了自然法则,该权利要求还描述了从人类患者获得血浆样品的步骤(步骤a),和检测样本中JUL-1的存在的步骤(步骤b)。当单独考虑时,与上述权利要求1类似的原因,步骤a和b本身是常规活动。然而,该权利要求进一步包含了向所诊断患者局部施用有效量的维生素D的额外要素(步骤d)。维生素D是已知的产品,在本申请之前,其通常用作口服补充剂来维持骨骼健康。由于局部施用维生素D并不是在领域内广泛流行的方法,所以局部使用维生素D是一个非常规的步骤。因此,局部施用维生素D治疗julitis不是本领域人员常规做法的常规步骤。无论是单独考虑还是与其他额外元素综合考虑,局部使用维生素D的步骤总体上远远超过了司法例外的情况(步骤2B:是)。因此权利要求4属于可专利主题。
五、应对策略和建议
结合"两步法"测试和以上示例可以看出,对于涉及天然产物的专利申请来说,如果想要使权利要求通过101法条的测试,可以从"额外元素"和"明显区别技术特征"两个方面双管齐下。首先,在撰写新申请阶段,应当结合发明的关键技术点和实际的商业应用场景,在权利要求中布局各种不同主题的产品独立权利要求,并且,在相应主题的独立权利要求下布局一系列包含不同"额外元素"的从属权利要求。同时,在说明书中,可以详细描述所要求保护的产品在包含了各种额外元素之后,与对应的天然产物相比,具有哪些明显区别特征,实现哪些突出技术效果(例如,结构、功能或其他方面的改进),避免相关额外元素被认为是常规技术,未超出司法例外情况。其次,在答复审查意见阶段,应当根据具体案情,对权利要求进行合理修改(必要时,引入适当的"额外元素"),并结合说明书中的关于"额外元素"的描述,对修改后的权利要求的专利适格性予以充分论述。在一些情况下,还可以引用合适的审查指南示例或在先法院判例,进一步支持或佐证相关论述。
而对于涉及诊断方法的专利申请来说,鉴于司法例外自然法则的特殊性,"额外元素"的存在显得尤为重要。因此,在撰写新申请阶段,应当深入分析发明的关键技术点和实际商业应用场景中可能涉及的各种"额外元素"(最理想的情况下,实际商业应用场景中不可避免必须使用的额外元素),从不同角度和层次审慎考虑和布局各种方法权利要求。例如,可以在诊断方法的基础上,考虑引入非常规的检测试剂或新开发的检测试剂,或者引入特定检测步骤或其他额外步骤(例如,治疗该疾病的药物和/或治疗步骤),以期利用相关"额外元素"克服101法条的挑战。在这种情况下,建议在说明书中对各种额外元素(包括检测试剂、检测步骤、治疗药物、治疗步骤)进行详细描述,这对于后续在审查阶段中的论述和争辩是特别有利的。
上文已针对生物医药领域中不同类型的权利要求主题,提供了克服101法条挑战的常见应对策略和应对方案。从目前的美国专利审查实践来看,超出司法例外的"额外元素"基本上是克服101法条挑战(特别是在涉及自然现象/自然产物/自然法则司法例外的情况下)所必需的。换言之,这些应对方案基本上都需要在核心的发明点或者说原本所意欲保护的最宽保护范围的基础上添加"额外元素"。而"额外元素"的引入不可避免会导致权利要求牺牲一部分保护范围,这势必会或多或少地影响到专利授权后的可维权性和授权专利的价值。因此,在101法条现行的审查实践下,申请人/权利人都面临着以下挑战:
(1)是否能够巧妙地挑选和设计"额外元素",而不实质性影响权利要求的保护范围;以及,
(2)如果无法实现第(1)点,如何在保护范围中进行合理的取舍(即,引入哪些"额外元素"),使得牺牲的保护范围不会严重影响授权专利的价值,或者使得牺牲一部分保护范围后获得授权的专利对于申请人/权利人来说仍然是"好用"的(例如,仍然能够有效限制竞争对手而不会被轻易地规避)。
对于不同的申请人、不同的技术领域、不同的具体案情来说,"好用"的专利并不是一概而论的。专利战略服务于商业战略。在不同情况下,"好用"的专利也许是能够有效阻止竞争对手商业行为的专利(例如,容易界定侵权行为,容易取得侵权证据的专利),也可能是能够使申请人在一定时间内享有独占权从而提高其市场竞争力的专利(即,覆盖了足够的范围以使得竞争对手难以规避的专利),还可能是能够快速授权并帮助其在产品上市前在全球范围内进行宣传的专利。例如,更新迭代速度快的快消品企业和"十年磨一剑"的医药企业在"好用"的专利的评价标准上显然会有所不同。因此,在应对101法条挑战时,在"额外元素"的取舍上,申请人/权利人应当充分考虑自身的商业战略和实际需求,审慎进行选择。
综上,101法条所带来的难题并不存在绝对的最优解。申请人/权利人应当综合考虑自身商业需求以及实际的案情,制定最适合自己的应对方案。鉴于101法条的独特性和复杂性,申请人/权利人应当在撰写和提交申请之前予以充分考虑,提前设计和制定应对方案,必要时,咨询专业的专利代理机构和专利代理师的意见,为自己争取最合适的专利保护。
1. USPTO. Interim Guidance on Patent Subject Matter Eligibility (16 December 2014).
2. USPTO. 2019 Revised Patent Subject Matter Eligibility Guidance (2019 PEG).
3. USPTO. The October 2019 Update: Subject Matter Eligibility (October 2019 Update).
4. Association for Molecular Pathology v. Myriad Genetics, Inc., 569 US 576 (2013).
5. USPTO. 35 USC § 101: Statutory Requirements and Four Categories of Invention (August 2015).
6. Fitzgerald M J, Spek E J. Microbiome therapeutics and patent protection [J]. Nature Biotechnology, 2020, 38(7): 806-810. DOI: 10.1038/s41587-020-0579-z.
7. Chang B C, Wang S J. The impact of patent eligibility on biotech patents: A flow chart for determining patent eligibility and an immune therapy case study [J]. Human Vaccines & Immuno therapeutics, 2015, 11(3): 789-794. DOI: 10.1080/21645515.2015.1009344.
8. Webber P. The end of DNA patents in the United States? [J]. Expert Opinion on Therapeutic Patents, 2013, 23(12): 1525-1527. DOI: 10.1517/13543776.2013.849245.
The content of this article is intended to provide a general guide to the subject matter. Specialist advice should be sought about your specific circumstances.


